Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
1-хлорпропан-2-он
Синонимы и иностранные названия:
1-хлор-2-пропанон (рус.)
хлорацетон (рус.)
Тип вещества:
органическое
Внешний вид:
бесцветн. жидкостьБрутто-формула (по системе Хилла для органических веществ):
C3H5ClOФормула в виде текста:
CH3COCH2ClМолекулярная масса (в а.е.м.): 92,52
Температура плавления (в °C):
-44,5Температура кипения (в °C):
119Температурные константы смесей (содержание в весовых процентах):
109,2 °C (температура кипения азеотропа, давление 1 атм) 1-хлорпропан-2-он 28,5% метилбензол 71,5%
Растворимость (в г/100 г растворителя или характеристика):
вода: 8,257 [Лит.]
диэтиловый эфир: растворим [Лит.]
хлороформ: растворим [Лит.]
этанол: растворим [Лит.]
Плотность:
1,15 (20°C, г/см3, состояние вещества - жидкость)
Некоторые числовые свойства вещества:
Минимальная раздражающая концентрация в воздухе (человек, мг/л): 0,018
Непереносимая раздражающая концентрация в воздухе (человек, мг/л): 0,11
Метод получения 1:
Источник информации: Buchman, E.R., Sargent, H. (1945). Thiamin Analogs. III. 4-Methyl-5-(hydroxymethyl)-thiazole / Journal of the American Chemical Society. - 1945. - Vol. 67, No. 3 стр. 401 [doi: 10.1021/ja01219a013]CH3COCH3 + SO2Cl2 → CH3COCH2Cl + SO2 + HCl
К 2320 г (2900 мл; 40 мол.) х. ч. ацетона в колбе, погружённой в баню со льдом, прибавляют из капельной воронки 320 г (2,37 мол.) хлористого сульфурила. Прибавление ведут при непрерывном перемешивании и медленно, затрачивая на всю операцию 5,5 часов. Реакционную массу предохраняют от попадания влаги.
По внесении всего хлористого сульфурила смесь упаривают при пониженном давлении для удаления избытка ацетона. Остаток промывают водным раствором поташа, сушат сернокислым натрием (примечание) и фракционируют.
Выход: 158 г (72% на хлористый сульфурил) хлорацетона, вполне свободного от более охлорённых производных. Продукт кипит между 118 и 120° и имеет d(15/4) 1,135 и d(25/4) 1,123.
Примечание
Хлорацетон, по-видимому, образует нераздельнокипящую смесь с ацетоном и водой.
(Перевод с англ. Bitrex)
Метод получения 2:
Источник информации: Van Atta, R.E., Zook, H.D., Elving, P.J. Synthesis of Monochloroacetone / Journal of the American Chemical Society. - 1954. - Vol. 76, No. 4 стр. 1186 [doi: 10.1021/ja01633a086]CH3COCl + 2CH2N2 → CH3COCHN2 + CH3Cl + N2
CH3COCHN2 + HCl → CH3COCH2Cl + N2
В 1-литровую трёхгорлую колбу помещают безводный эфирный раствор объёмом около 500 мл, содержащий 21 г (0,5 мол.) диазометана. Раствор охлаждают и медленно прибавляют из капельной воронки 19,6 г (0,25 мол.) хлористого ацетила, непрерывно перемешивая и не давая температуре подняться выше 5°. По внесении всего хлористого ацетила реакционную массу оставляют стоять на 2 час., после чего её насыщают сухим хлористым водородом в течение 2 час.
Большую часть эфира удаляют перегонкой. Оставшийся раствор фракционируют с небольшим дефлегматором.
Выход: 15,8 г (68% на взятый хлористый ацетил) хлорацетона, кипящего при 118—119°/736 мм. Продукт имеет d(25/4) 1,1260.
Хлор: найдено 38,4, вычислено 38,3 (C3H5OCl).
(Перевод с англ. Bitrex)
Метод получения 3:
Источник информации: Kochi, J. K. The Reduction of Cupric Chloride by Carbonyl Compounds / Journal of the American Chemical Society. - 1955. - Vol. 77, No. 20 стр. 5275 [doi: 10.1021/ja01625a016]CH3COCH3 + 2CuCl2 → CH3COCH2Cl + Cu2Cl2 + HCl
Раствор 12 г двухводной хлорной меди и 6 г хлористого лития в смеси 150 мл ацетона и 50 мл воды кипятят с обратным холодильником в течение 24 часов и затем быстро перегоняют. Фракцию, кипящую между 56 и 100°, фракционируют на 150-сантиметровой колонке с вакуумной рубашкой и спиральной насадкой для удаления ацетона. Слезоточивый кубовый остаток объёмом около 15 мл по охлаждении разделяется на два слоя. Его центрифугируют, нижний маслянистый слой отделяют и перегоняют на 50-сантиметровой спиральной колонке с вакуумной рубашкой, получая две фракции: I, кипящую при 89°, и II, кипящую при 118°. Фракция I по охладжении разделяется на два слоя — хлорацетон и воду в отношении приблизительно 5:1, а фракция II представляет собой чистый хлорацетон. Динитрофенилгидразоны, полученные из обеих фракций, не дают депрессии температуры плавления при смешении с заведомым образцом динитрофенилгидразона хлорацетона (125—126°).
Выход хлорацетона около 3,3 г (60%).
(Перевод с англ. Bitrex)
Метод получения 4:
Источник информации: Вейганд-Хильгетаг Методы эксперимента в органической химии. - М., 1968 стр. 1802CH3COCH3 + 2Cl2 + CaCO3 → 2CH3COCH2Cl + CaCl2 + CO2 + H2O
В колбу загружают 500 г ацетона и 125 г измельченного в порошок мрамора. Охлаждают проточной водой и пропускают в реакционную массу умеренный ток хлора при этом добавляя по каплям 315 мл воды. Температура реакционной смеси должна быть не выше 30 °С и не ниже 10 °С. После растворения почти всего мрамора температуру повышают до 40 °С и поддерживают ее в течение нескольких часов до окончания выделения CO2. Следят за тем, чтобы в смеси все время оставался мрамор, в случае надобности его добавляют в небольшом количестве. По окончании реакции отделяют в делительной воронке образовавшийся верхний слой и подвергают его фракционной перегонке, собирая продукт с температурой кипения 118-120 °С.
Метод получения 5:
Источник информации: Патент США US2,209,683 (от 27.06.1936). Halogenation of diketene
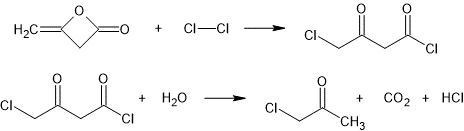
В 25 г (0,297 мол.) дикетена при температуре от 0 до 10° пропускают 21 г (0,296 мол.) сухого хлора. Реакционную массу выливают в 150 мл холодной воды и кипятят с обратным холодильником в течение 2 часов. В ходе реакции выделяется углекислый газ и отслаивается хлорацетон. Массу оставляют охлаждаться на ночь.
Смесь трижды экстрагируют эфиром, эфирные экстракты сушат хлористым кальцием и фракционируют при атмосферном давлении.
Выход: 19,1 г (около 70% теоретич.) хлорацетона с т. кип. 117—121°.
(Перевод с англ. Bitrex)
Метод очистки или выделения из смесей 1:
Источник информации: Armarego W. L. F. Purification of Laboratory Chemicals. - 7ed. - 2013 стр. 115Водный раствор хлорацетона встряхивают с малыми порциями диэтилового эфира, который экстрагирует преимущественно 1,1-дихлорацетон. Затем хлорацетон экстрагируют большим количеством эфира и перегоняют в неглубоком вакууме. Его сушат хлористым кальцием и хранят при охлаждении сухим льдом. Хлорацетон также можно настоять над безводным сернокислым кальцием, перегнать и хранить над безводным сернокислым кальцием.
Способы получения:
- Хлорацетон получается реакцией хлора, ацетона и мрамора в присутствии воды. Осторожной реакцией хлора с большим избытком ацетона (1:5) и мрамора в присутствии воды при температуре от 5 до 10 С можно получить хлорацетон, не содержащий 1,1-дихлорацетона по данным рамановской спектроскопии. [Лит.1
 , Лит.2
, Лит.2 ]
]
2CH3COCH3 + 2Cl2 + CaCO3 → 2CH3COCH2Cl + CaCl2 + CO2 + H2O
- Хлорацетон можно получить гидролизом 2-метил-2-(хлорметил)-1,3-диоксолана (этиленкеталя хлорацетона) избытком 1% соляной кислоты при кипячении. Этиленкетали хлорацетона и 1,1-дихлорацетона можно разделять фракционной перегонкой. [Лит.1]
Используется для синтеза веществ:
(RS)-1-хлорпропан-2-ол
2-метил-2-(хлорметил)-1,3-диоксолан
4-метилтиазол
Реакции вещества:
- Реагирует с 4-хлорфенилмагнийбромидом с образованием 1-хлор-2-(4-хлорфенил)пропан-2-ола. [Лит.]
- Реагирует с 2-метоксифенилмагнийбромидом с образованием 1-хлор-2-(2-метоксифенил)пропан-2-ола. [Лит.]
- При действии на хлорацетон в диэтиловом эфире гидроксида калия образуется пропионат калия. Название реакции: перегруппировка Фаворского. [Лит.1]
CH3COCH2Cl + 2KOH → CH3CH2COOK + KCl + H2O
- При нагревании хлорацетона с 3 молями фенола и дымящей соляной кислотой образуется 1,2,2-трис(гидроксифенил)пропан. [Лит.1]
CH3COCH2Cl + 3C6H5OH → (HOC6H4)2C(CH3)CH2C6H4OH + H2O + HCl
- При действии на хлорацетон бромида 4-метоксифенилмагния образуется 1,2-ди(4-метоксифенил)пропен. [Лит.1, Лит.2
 ]
]
CH3COCH2Cl + 2CH3OC6H4MgBr → CH3OC6H4CH=C(C6H4OCH3)CH3 + MgBr2 + MgOHCl
- При действии на хлорацетон бромида 4-этоксифенилмагния образуется 1,2-ди(4-этоксифенил)пропен. [Лит.1, Лит.2
 ]
]
CH3COCH2Cl + 2C2H5OC6H4MgBr → C2H5OC6H4CH=C(C6H4OC2H5)CH3 + MgBr2 + MgOHCl
- 1-Хлор-2-пропанол может быть получен восстановлением хлорацетона борогидридом натрия. Выход 85%. [Лит.1]
- Иодацетон получают реакцией хлорацетона или бромацетона с иодидом калия. [Лит.1]
Некоторые нечисловые свойства вещества:
перегоняется с водяным паром
Аналитические реакции вещества:
- реагент: ванилин в смеси концентрированных серной и соляной кислот; результат реакции: красн. окрашивание, постепенно переходящее в сине-зеленое или зеленовато-черное. При кипячении на водяной бане сразу появляется синяя окраска.
Источники информации:
- Yalkowsky S.H., Yan H., Jain P. Handbook of aqueous solubility data. – 2nd ed. - CRC Press, 2010. - С. 52
- Вредные вещества в промышленности: Справочник для химиков, инженеров и врачей. - 7-е изд., Т.1. - Л.: Химия, 1976. - С. 547
- Справочник химика. - 2 изд., Т. 2. - Л.-М.: Химия, 1964. - С. 910-911
- Успехи химии. - 1935. - Т.4, №8. - С. 1276-1282
- Франке З. Химия отравляющих веществ. - Т.1. - М.: Химия, 1973. - С. 80
- Химический энциклопедический словарь. - Под ред. Кнунянц И.Л. - М.: Советская энциклопедия, 1983. - С. 658
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер